나노젠 관계자는 "임상시험을 통해 과학적 증거에 따라 나노코박스에 대한 긴급 허가를 신청했다"고 밝혔다.
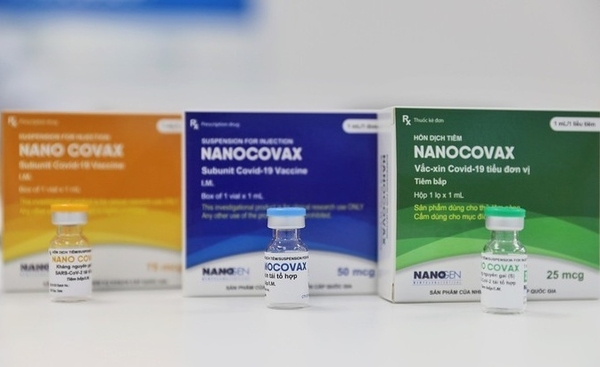
23일 오전 익명을 요구한 나노젠 대표는 "나노코박스의 응급면허 신청 근거는 군의관학교와 호찌민시 파스퇴르연구소의 보고서를 근거로 했다"고 밝혔다. 이들은 지난 두 차례의 임상시험에서 백신을 평가한 독립단위 2곳이다.
나노젠은 최근 총리에게 나노코팍스 백신에 대한 긴급 허가 승인을 요청했다. 나노젠 대표는 응우옌탄롱 보건부 장관에게도 긴급 면허 신청서를 보냈다고 말했다. 하지만 보건부는 나노코박스의 긴급허가를 받을 만한 과학적 근거가 충분하지 않다고 평가했다.
나노코팍스 백신은 임상 3단계에 있으며 이번 주 초까지 1,000명 이상이 첫 주사를 맞았다. 임상 3단계 에 참여할 것으로 예상되는 인원은 모두 13,000명이다.
나노젠의 보고에 따르면 나노코박스의 면역력은 99.4%로 세계 다른 백신에 비해 크게 떨어지지 않는다. 임상 1상 및 2상의 중간 결과는 윤리 위원회, 보건부가 잘 승인하고 평가했다.
"우리는 미국 웹사이트 ClinicalTrial.gov를 포함하여 전세계에 임상시험을 발표했다. 세계보건기구(WHO)는 나노코박스의 임상시험 정보와 효능 측정 가이드라인을 모두 기록해 백신 나노젠의 효과적인 보호는 이 지침을 따랐다고 밝혔다.
그는 "백신은 긴급 인허가용으로 충분한 과학적 자료가 있다"며 "허가되면 수출이 아닌 베트남 국민의 요구에 맞는 백신 생산에 주력할 것"이라고 말했다.
하지만, 보건부 관계자는 나노코박스의 백신이 "긴급 허가를 위한 과학적 근거가 충분하지 않다"고 확인했다.
긴급상황에 대한 코비드-19 백신의 사용허가는 유행성 질환으로 인해 평소처럼 장기간 백신을 감시할 시간이 부족하다. 하지만, 안전성을 보장하기 위해, 백신은 여전히 보호 효과를 평가하는 모든 과정을 거쳐야 한다고 보건부는 말한다.
국제 관행에 따르면, 긴급하게 사용되기 전 모든 코비드-19 백신은 3단계 임상 시험을 준수해야 하며, 안전, 면역성 및 가장 중요한 효능 보호의 3가지 요소를 보장해야 한다.
베트남은 전염병 예방의 긴급한 필요성으로 지금까지 화이자 코모르네티(미국), 아스트라제네카(영국), 가말라야의 스푸트니크-V(러시아), 시노팜의 베로셀(중국) 등 4개 백신을 긴급 허가했다. 모더나 백신은 허가 과정 중에 있다.
보건부에 따르면 위의 모든 백신은 긴급 승인을 받기 전에 3단계 임상시험을 거쳤다. 3상 임상시험 규모는 2만~5만명이다. 특히 아스트라제네카 백신은 11개국에서 4만9626명이 참여한 가운데 3상을 했다. 시노팜의 베로셀 백신은 6개국에서 4만5000명이 넘게 시험했다. 백신 스푸트니크-V는 5개국에서 2만만1977명을 주사했다. 화이자는 6개국 4만3418명, 모더나는 4개국 3만420명을 테스트했다.
보건부 장관은 3단계는 백신 안전성과 보호효과 평가를 목표로 대규모로 진행돼야 한다고 말했다.
안전성, 면역성을 테스트하고 최적의 투여량을 결정하기 위해 1, 2단계 임상시험을 여러 그룹에서 소규모로 수행하였다. 1단계와 2단계에서의 면역성 평가는 급한 승인을 위한 결정적인 요소가 아니다.
그는 "3상 임상시험 결과만 이 백신이 보호에 효과가 있는지, 코비드-19의 위험을 줄이는지, 질병을 완화하는지를 평가하는 결정적인 요소가 될 것"이라고 말했다.
-VN익스프레스
▶관련기사: https://www.goodmorningvietnam.co.kr/news/article.html?no=42204